You are here
Ensayo clínico para personas con síndrome del intestino irritable (SII) y diarrhea
Para este ensayo clínico, los investigadores están seleccionando personas con «síndrome del intestino irritable con predominio de diarrea (SII-D)».
El SII-D es un trastorno de la función gastrointestinal caracterizado por dolor abdominal, hinchazón y diarrea (heces sueltas o líquidas).
Nota: el SII-D no es una enfermedad inflamatoria intestinal (EII) como la enfermedad de Crohn o la colitis ulcerosa.
El objetivo principal de este estudio clínico es ver si un fármaco nuevo puede aliviar los síntomas del SII-D (dolor abdominal, hinchazón y diarrea) en los pacientes. El ensayo clínico durará un máximo de 15 semanas.
Si está interesado en este estudio, póngase en contacto con su médico de cabecera o especialista para hablar acerca de la posible participación y solicite una derivación a uno de los centros de estudio participantes.
El CE/AH autorizó la realización de este estudio el 14/11/2019. Esta autorización es válida para todos los centros participantes en España. Este estudio está patrocinado por Cosmo Technologies.
¿Qué es el "síndrome del intestino irritable con predominio de diarrea (SII-D)"?
El síndrome del intestino irritable (SII) es un trastorno intestinal funcional del tracto gastrointestinal, lo que significa que el intestino no funciona de manera óptima.
El SII se caracteriza por dolor abdominal y malestar recurrente junto con una alteración de la función intestinal (diarrea, estreñimiento o la combinación de ambas) que habitualmente dura meses o años.
El SII no es una enfermedad inflamatoria intestinal (EII) como la enfermedad de Crohn o la colitis ulcerosa.
Para este estudio, los investigadores están seleccionando personas con el subtipo específico de síndrome del intestino irritable con predominio de diarrea (SII-D).
Las personas con SII-D padecen dolor abdominal, hinchazón y diarrea (heces sueltas o líquidas).
Las personas que sufran principalmente estreñimiento no son elegibles para este estudio.
¿Cuál es el objetivo de este ensayo clínico?
Se ha demostrado que el SII-D tiene un impacto negativo significativo en la calidad de vida relacionada con la salud.
El objetivo principal de este estudio es ver si un fármaco nuevo puede ayudar a las personas con SII-D.
Este estudio evalúa si el tratamiento con el fármaco en estudio puede disminuir el dolor abdominal y cambiar la consistencia de las heces.
¿Qué fármaco en estudio se está investigando?
El fármaco en estudio es un antibiótico oral. Un antibiótico es un agente con acción antibacteriana, es decir, que su acción está dirigida a eliminar bacterias específicas en el intestino.
El fármaco en investigación en este ensayo clínico es una nueva formulación (comprimido) de un antibiótico que ya está autorizado y comercializado. El objetivo del comprimido es eliminar bacterias específicas en el intestino. Esta nueva formulación permite una administración máxima del principio activo en el intestino, lo que produce un efecto optimizado. La absorción del fármaco del estudio en sangre, de hecho, es insignificante, lo que limita el efecto en el tracto gastrointestinal
El fármaco del ensayo se administra directamente en el colon y evita efectos indeseados sobre la flora bacteriana beneficiosa que vive en zonas superiores del tracto gastrointestinal.
El antibiótico que se investiga en este estudio ha estado disponible en el mercado estadounidense durante más de una década para tratar la diarrea del viajero. Con los resultados de este estudio, el patrocinador tiene como objetivo ampliar las indicaciones del fármaco con una nueva formulación para el SII-D en Europa.
¿Quién puede participar?
Cerca de 342 pacientes participarán en este estudio, de los cuales 92 en España.
Para participar, los pacientes deben cumplir los requisitos siguientes:
- Tener por lo menos 18 años
- Tener dolor o molestias abdominales recurrentes desde hace, al menos, 6 meses
- Dolor en cualquier parte del abdomen, por lo menos, 1 día a la semana (en los últimos 3 meses)
- Presentar síntomas activos de SII-D:
- dolor abdominal
- hinchazón
- consistencia de las heces de diarrea leve/grave (heces del tipo 6 o 7; consulte la imagen)
- Por lo menos 3 evacuaciones intestinales a la semana
- Haberse sometido a una colonoscopia en los últimos 5 años (o en los últimos 2 años si el paciente tiene más de 50 años), o estar dispuesto a someterse a una colonoscopia como parte del proceso de selección
Las condiciones siguientes excluyen la participación de los pacientes:
- Embarazo, lactancia o planes de quedarse embarazada durante el desarrollo del estudio.
- Participación en otro ensayo clínico durante la duración este ensayo clínico.
- Estreñimiento predominante
- Enfermedad de Crohn, colitis ulcerosa, VIH, SIDA, pancreatitis, diabetes
- Consumo excesivo de alcohol o drogas
Tenga en cuenta que esta lista no es exhaustiva. Hable con su médico de cabecera o especialista para determinar si reúne los requisitos para participar en el estudio y solicitar una derivación a uno de los centros de estudio participantes. Todos los exámenes realizados como parte del estudio se llevarán a cabo en el centro del estudio bajo la supervisión de un médico del estudio. El médico del estudio le informará si usted reúne las condiciones para participar en este estudio.
La participación en el estudio es totalmente voluntaria y puede detenerse en cualquier momento.
¿Qué debo hacer si estoy interesado en el estudio?
- Hable con su médico de cabecera o especialista acerca del estudio y muéstrele la información disponible en el sitio web del estudio.
- Pregúntele a su médico de cabecera o especialista si reúne los requisitos para participar en el estudio
- Solicite a su médico de cabecera o especialista una derivación a uno de los centros de estudio participantes, enumerados en «¿Qué centros del estudio participan en el ensayo clínico?»
¿Cuántas veces tendrá que visitar el centro del estudio?
El médico del estudio decidirá si usted reúne las condiciones para participar en este ensayo y le pedirá que firme un documento de consentimiento informado.
Si se autoriza su participación en el estudio y usted desea participar, primero, entrará en un periodo de selección del estudio (visita 1). En ese momento, el médico del estudio recopilará información para determinar si puede iniciar el tratamiento.
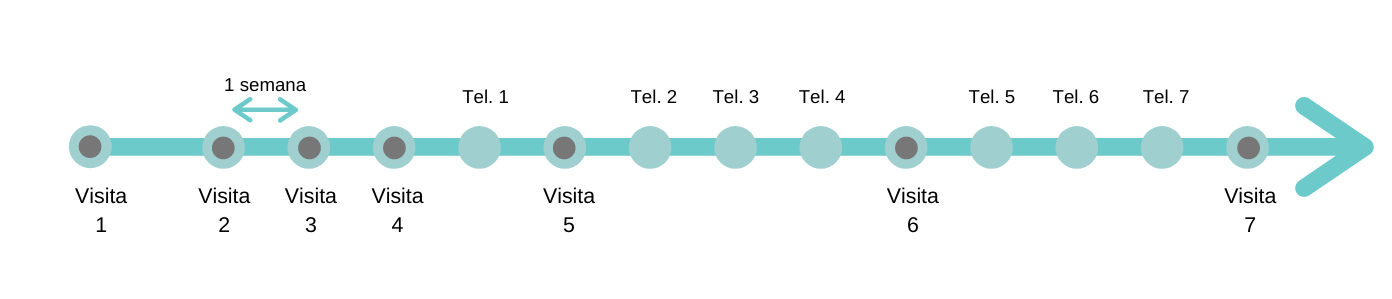
Su participación durará un máximo de 15 semanas, e incluye:
- 7 visitas al centro del estudio
- 7 llamadas telefónicas
En el estudio hay tres pautas de tratamiento posibles. Se le asignará de forma aleatoria (como a cara o cruz) para recibir una de las tres opciones de tratamiento. Se le administrará tratamiento durante 14 días consecutivos. Existe una probabilidad de 1/3 de recibir solamente placebo.
¿Cuáles son los posibles beneficios y riesgos de participar?
Como en cualquier ensayo clínico y procedimiento médico estándar hay riesgos para el paciente. Antes de que decida participar, el equipo del estudio le explicará el ensayo clínico y los posibles riesgos/inconvenientes. Tendrá la oportunidad de formular preguntas.
¿Qué centros del estudio participan en el ensayo clínico?
- Hospital Universitari Vall d'Hebron - Dr. Javier Santos, Ed.Recerca - Mediterrània | Planta Baixa - Lab 016, Passeig Vall d'Hebron, 119-129, 08035 Barcelona
- Hospital Universitari Germans Trias i Pujol (Can Ruti) - Dr. Jordi Serra, Servicio de Aparato Digestivo Carretera de Canyet, s/n 08916 Badalona, Barcelona
- Hospital de Viladecans - Dr. Maria Antonia Perelló Juan, Av. de Gavà, 38, 08840 Viladecans, Barcelona
- Hospital Univ. General de Catalunya - Dr. Esteban Saperas, Carrer Pedro i Pons, 1, 08195 Sant Cugat del Vallès, Barcelona
¿Qué métodos anticonceptivos se permiten?
Tomar el fármaco del estudio puede suponer riesgos desconocidos para mujeres embarazadas y para el embrión, el feto (niño no nacido) o el lactante. Actualmente se desconocen cuáles son esos riesgos. Por lo tanto, es importante que utilice un método anticonceptivo eficaz durante su participación en este estudio.
Los métodos anticonceptivos eficaces para mujeres son:
- Anticonceptivos hormonales orales, implantables, transdérmicos o inyectables, a partir de al menos dos meses antes de la visita de selección;
- Un dispositivo intrauterino (DIU), preservativo femenino con espermicida, esponja anticonceptiva con espermicida, diafragma con espermicida o capuchón cervical con espermicida, a partir de al menos dos meses antes de la visita de selección;
- Una pareja sexual masculina que consienta usar el preservativo masculino con espermicida;
- Una pareja sexual estéril
- Abstinencia
Los métodos anticonceptivos eficaces para hombres son:
- Ser estéril o tener una pareja sexual estéril;
- Preservativo masculino con espermicida;
- Abstinencia
¿Hay compensación para los participantes?
No se les cobrará por participar en el estudio. El fármaco del estudio, los procedimientos del estudio y las visitas del estudio se facilitarán a los pacientes de forma gratuita. Durante la participación en el estudio, los pacientes todavía necesitarán recibir atención médica regular. Los pacientes (y/o el proveedor sanitario) tendrán que pagar los costes de la atención médica regular que no sean parte de este estudio.
El patrocinador del estudio ha establecido reembolsar los costes de desplazamiento (importe fijo) derivados de la participación en este estudio. El equipo del estudio le facilitará más información.